Đường uống là con đường điển hình để đưa thuốc vào cơ thể, nhưng những nhược điểm như chuyển hóa lần đầu, chi phí cao và liều dùng lặp lại khiến cho con đường này trở nên đầy thách thức. Cần phải phát triển một cơ chế đưa thuốc mới để tăng cường hiệu quả điều trị, ổn định và bảo vệ thuốc để giải quyết tất cả những thách thức này ( Shaw và Mitchell, 1983 ).
Phân phối thuốc qua da là một con đường đưa thuốc đã được thiết lập, được biết là có tác dụng tăng cường hiệu quả điều trị, dễ dàng đưa thuốc vào cơ thể và cho phép ngừng điều trị ngay lập tức nếu cần . Con đường đưa thuốc này bỏ qua quá trình chuyển hóa ở gan để đạt đến tuần hoàn toàn thân, dẫn đến tăng khả dụng sinh học của thuốc. Hơn nữa, nó làm giảm tác dụng phụ của một số loại thuốc, ví dụ, thuốc chống viêm không steroid (NSAID), thường liên quan đến việc đưa thuốc vào đường tiêu hóa (GIT).
Cung cấp thuốc qua da để tuần hoàn toàn thân phù hợp với một số tình trạng lâm sàng, chẳng hạn như tăng huyết áp, viêm khớp, tiểu đường, ung thư và mức cholesterol trong máu cao. Vì liều dùng được đưa qua da và được duy trì trong thời gian dài thông qua các hệ thống đưa thuốc được thiết kế riêng, đặc biệt là trong trường hợp Nanoemulsion, nên việc cải thiện khả năng tuân thủ của bệnh nhân là vô cùng quan trọng.
Phân phối qua da cũng có ưu điểm so với tiêm dưới da, gây đau, tạo ra chất thải y tế nguy hiểm và gây ra nguy cơ lây truyền bệnh do tái sử dụng kim, đặc biệt là ở các nước đang phát triển 5 . Ngoài ra, các hệ thống qua da không xâm lấn và có thể tự thực hiện. Chúng có thể giải phóng trong thời gian dài (lên đến một tuần). Chúng cũng cải thiện khả năng tuân thủ của bệnh nhân và các hệ thống này thường không tốn kém.
Stoughton đã dự đoán về sự hấp thụ thuốc qua da từ rất lâu vào năm 1965, từ đó hình thành kỹ thuật cho hệ thống đưa thuốc tại chỗ/xuyên da (TDDS) (Idson, 1975 ). Thuốc qua hệ thống đưa thuốc tại chỗ/xuyên da (TDDS) cung cấp phổ mở rộng để áp dụng cho các hình dạng và kích thước khác nhau của các chế phẩm có một hoặc nhiều thành phần hoạt tính, khi được áp dụng trên toàn bộ da, có thể phân bố khắp cơ thể hoặc có thể hoạt động tại chỗ tại vị trí bôi thuốc.
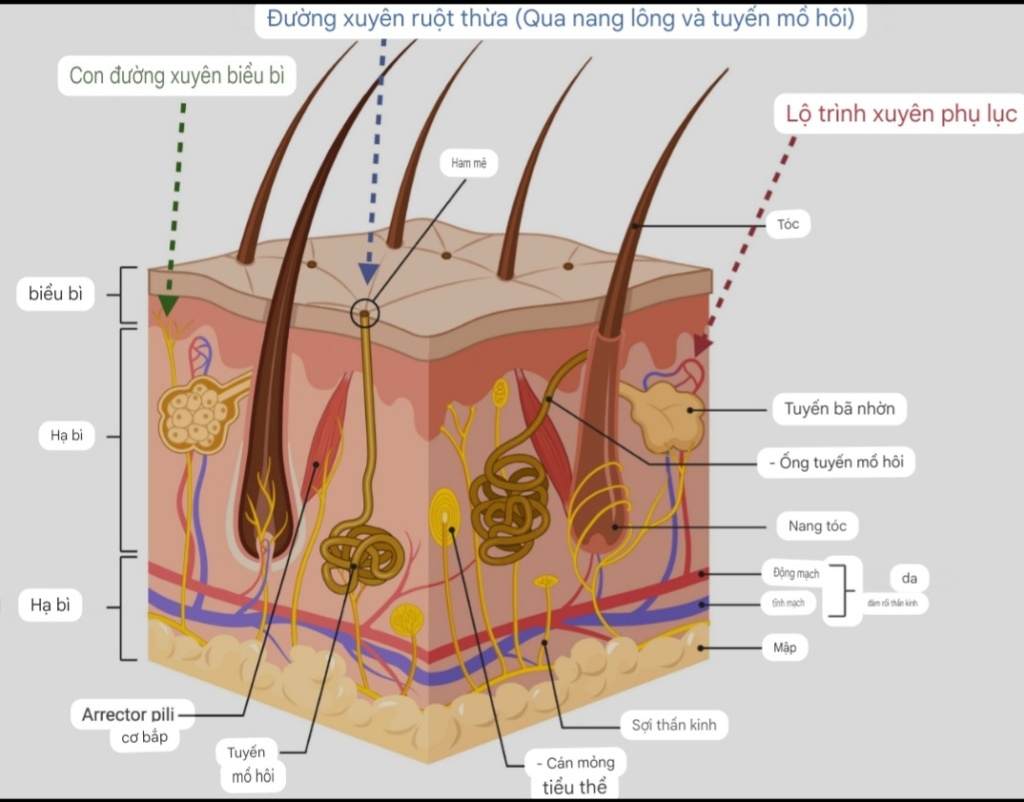
Lớp biểu bì trên diện rộng và chức năng không chính thức khiến da trở thành con đường lý tưởng để thuốc thâm nhập ( Prausnitz và Langer, 2008 ). Mặc dù vậy, các thử nghiệm quan trọng trong việc xây dựng hệ thống đưa thuốc tại chỗ/xuyên da (TDDS) là điều kiện tiên quyết để giải quyết lớp da bên ngoài sừng hóa, không thấm nước rất cao, ví dụ, ‘lớp sừng’ (SC) để chuyển dịch thành công sang các lớp bên dưới. Chức năng cốt lõi của lớp sừng là tạo ra một lớp bảo vệ cho các mô bên dưới da, tuy nhiên, chức năng phong tỏa này thường làm giảm lượng thuốc có thể di chuyển qua da một cách thụ động (Prausnitz và cộng sự, 2004 ).
Trong công nghệ hạt nano, phạm vi các hạt là 1–500 nm để chữa bệnh và chẩn đoán và đã khắc phục được vấn đề rất quan trọng là khả dụng sinh học thấp của thuốc. Đã có nhiều nghiên cứu mang tính đột phá và một số trong số chúng là các sản phẩm dựa trên công nghệ nano được cấp bằng sáng chế trong lĩnh vực y tế trong vài thập kỷ qua ( Boisseau và Loubaton, 2011 ).

Mục đích của kỹ thuật này là xác định và giải quyết các vấn đề về thuốc để tăng cường sức khỏe bằng cách giảm thiểu tác dụng phụ của thuốc với các phương pháp điều trị không xâm lấn. Các hạt nano cung cấp rất nhiều nguồn lực mới để đạt được những thành tựu này. Việc thay đổi thuốc và các thành phần khác ở quy mô nanomet thông qua các phương pháp tiếp cận công nghệ nano làm tăng đáng kể kết quả điều trị của các vật liệu này và làm giảm các tác dụng phụ liên quan. Diện tích bề mặt, nhắm mục tiêu vào vị trí, tăng cường độ hòa tan, phân phối kiểm soát và giải phóng kéo dài là một số tính chất phân biệt y học nano với các đối tác thông thường ( Hughes, 2005 ).
Lĩnh vực y học dựa trên vật liệu mang nano không ngừng phát triển và đã đạt được thành công trong việc chữa khỏi các bệnh ung thư và các bệnh truyền nhiễm vốn khó điều trị trong quá khứ ( Díaz-Torres và Vật liệu mang nano qua da, 2010 ).
Việc sử dụng các chế phẩm như vậy trên da vì lý do điều trị đã có từ lâu đời như lịch sử y học, tương tự như việc sử dụng thuốc mỡ và thuốc mỡ trong lịch sử liệu pháp truyền thống của Ai Cập và Babylon. Các mô hình lịch sử trong phân tích thẩm thấu được Lane và Hadgraft ( Hadgraft và Lane, 2005 ) mô tả rõ ràng. Trong nhiều thế kỷ, da đã phát triển một con đường quan trọng để đưa thuốc vào cơ thể để có tác dụng tại chỗ, hoặc toàn thân.
Tuy nhiên, da cũng là một trở ngại đáng kể và gây cản trở cho quá trình phân phối thuốc qua da. Trong khi đó, một số lượng hạn chế thuốc có thể tiếp cận lớp sừng ở nồng độ thích hợp để đạt được lượng thuốc hoạt động trong máu. Nhiều phương pháp đã được phát triển và cấp bằng sáng chế để tăng cường khả năng hấp thụ thuốc qua da ( Barry, 2001 ; Rizwan và cộng sự, 2009 ). Bảng 1 nêu bật những ưu điểm và nhược điểm chính của TDDS ( Escobar-Chávez và cộng sự, 2012 ).
Tài liệu:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2700785/
https://duocdainam.vn/xu-huong-y-khoa/cong-nghe-bao-che-than-thien
